亚洲食品添加剂法规差异:出口前最容易踩坑的几个点
摘要
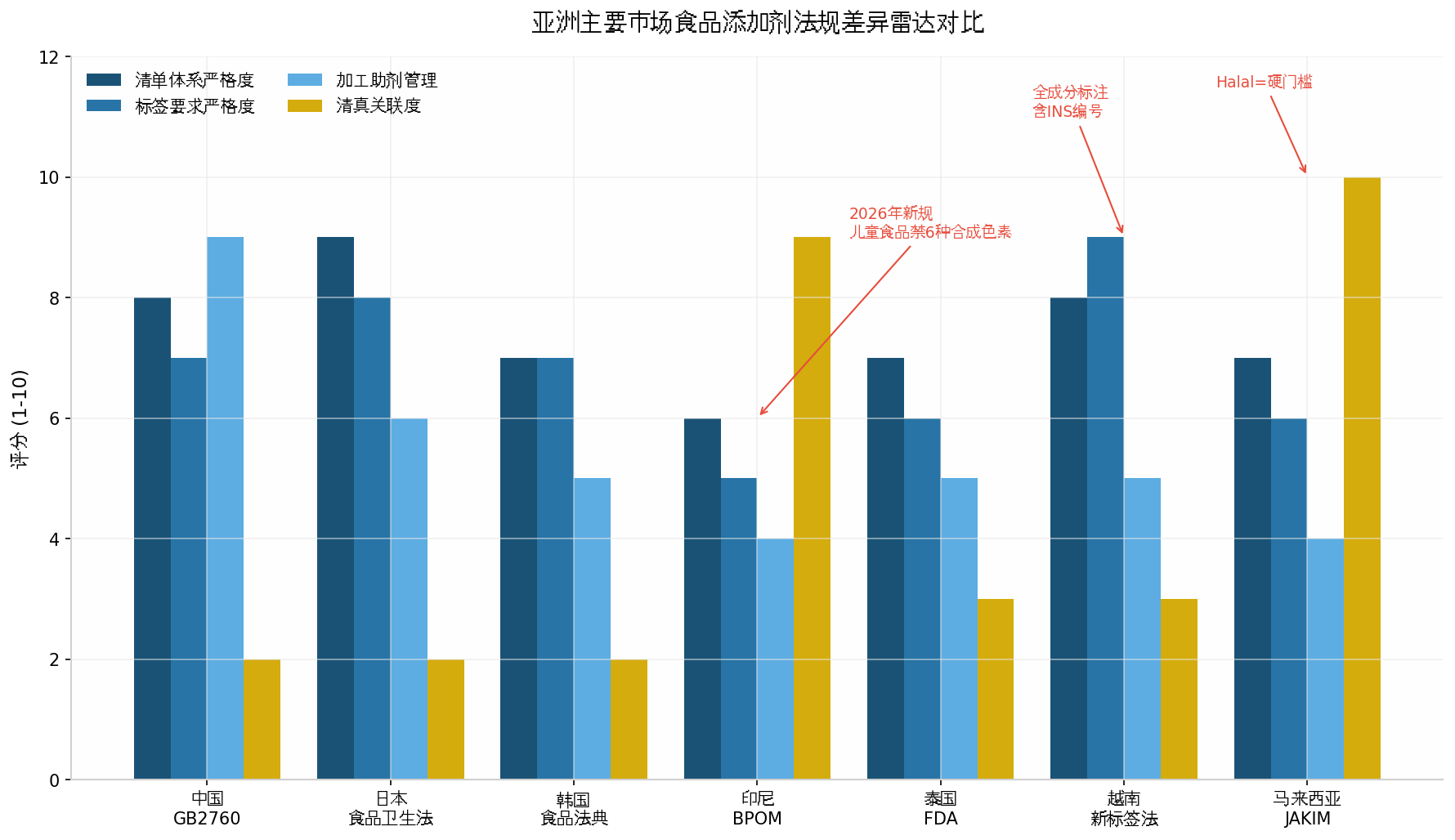
亚洲食品添加剂法规表面上都像“正面清单 + 限量管理”,但定义、标签、加工助剂、营养强化剂和认证路径差异很大。出口企业如果只按国内配方判断,很容易在日本、韩国、越南、印尼或马来西亚遇到禁用、重申报或标签不合规问题。
关键要点
- 中国、日本、韩国的清单体系不同,加工助剂和营养强化剂的管理逻辑也不同。
- 越南预包装食品要求全成分标注并包括添加剂 INS 编号,过渡期不能当作不用准备。
- TBHQ、D-阿洛酮糖等品种在不同国家的管理路径差异明显,不能用一个法规判断所有市场。
- 清真认证、动物源性载体、酒精溶剂、昆虫来源色素等,会影响印尼和马来西亚市场准入。
清单体系不同,合规判断就不同
中国 GB2760 采用正面清单和食品分类系统,添加剂按编号管理,每种添加剂对应允许使用的食品类别和最大使用量。日本有《指定添加剂清单》和《现有食品添加剂清单》,天然和化学合成添加剂都纳入正面清单控制。韩国食品法典与日本接近,但没有日本《现有食品添加剂清单》的等价物,加工助剂管理相对宽松。
加工助剂定义会改变标签和申报路径
中国、日本、韩国都把加工助剂纳入食品添加剂定义,但细节不一样。中国明确列出加工助剂,并区分“按生产需要适量使用”和只能在指定食品中用于指定功能的清单。日本则更多通过标签豁免来间接定义加工助剂。定义差异会导致同一款产品在不同国家的合规结论完全不同。
标签要求不是翻译问题
越南 2026 年 1 月颁布的新决议要求食品在上架销售前标明标准,预包装食品全成分标注包括添加剂 INS 编号,过渡期为 12-24 个月。日本在 1996 年法规修订后,使用天然食品添加剂的产品也必须在标签上注明。马来西亚要求双语标签,印尼进口食品标签审核周期经常拉长到三到六个月。
典型品种:TBHQ 和 D-阿洛酮糖
TBHQ 是典型案例。中国 GB2760 允许在月饼、饼干、方便米面制品等类别中使用,最大用量 0.2g/kg。但日本和一些欧盟国家已经禁用 TBHQ。出口日本的产品通常要换成维生素 E 等其他抗氧化方案。
D-阿洛酮糖也说明了管理路径差异。中国在 2025 年首次批准 D-阿洛酮糖为新食品原料;日本和韩国对 D-阿洛酮糖本身的申报要求不同,韩国 MFDS 在 2025 年 9 月发布新规,要求自 2026 年 10 月 1 日起,只能进口和使用经 MFDS 认证的酶制剂生产的阿洛酮糖产品。
清真认证和限量指标也会改变产品方案
马来西亚 JAKIM 和印尼 BPJPH 对添加剂来源审查严格。动物源性载体、酒精溶剂、昆虫来源色素,如胭脂虫红,都可能成为合规障碍。印尼和马来西亚正在推进认证互认,但落地时间表不明确,企业目前仍需要按两套体系准备。
基础指标也不能忽略。原文提到,碳酸饮料中铅限量在日本、韩国、中国和东盟之间存在差异。同一批产品,在中国合规,不代表在东盟就一定合规。出口前做目标市场预检测,比到港后被退运成本低得多。
出口前的实际做法
配方定型前先做合规预审,不要等产品完成后才发现某个添加剂在目标国禁用。建立“一国一配方”档案库,把允许清单、限量、标签、认证、检测指标和过渡期放在一起管理。对食品加工企业和添加剂客户来说,法规理解本身就是竞争力的一部分。